Die Eigenschaften, Struktur und Bedeutung der Zellulose
Chemisch: Cellulose (C6H10O5)n M = n x 162,142
Native Zellulose: 3 000 < n < 15 000
Technische Zellulose: 250 < n < 2 000
Bedeutung der Zellulose
Zellulose ist das Polysaccharid, das mengenmäßig am meisten vorkommt und gehört zu den Kohlenhydraten. Pflanzenfasern (Baumwolle, Flachs, Hanf) bestehen aus nahezu reiner Zellulose. Holz enthält etwa 50 M % Zellulose. Schilf und Stroh bestehen zu etwa 30 M % aus Zellulose.
Die Zellulose wird hauptsächlich in der Textil- und Papierindustrie, bei der Herstellung von Plasten, Sprengstoffen, Lacken, Verpackungsmaterialien als Wärme- und Schalldämmstoff sowie der Holzverzuckerung verwendet.
Struktur und Eigenschaften
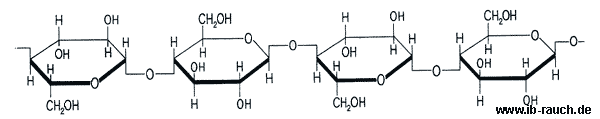
Zellulose besteht aus Glucosan- oder Glucan-Makromolekülen, in denen β-Glukosereste durch Sauerstoffbrücken in 1,4-Bindung verknüpft sind. Die Festigkeit und Elastizität der Zellulosefasern hat ihre Ursachen in der Molekülform der Makromoleküle, die in langen Fäden parallel zueinander liegen. Die Ketten der Makromoleküle von Zellulose sind unverzweigt.
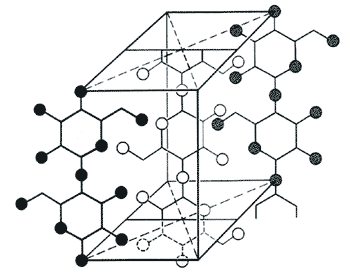
Zellulose besteht aus stäbchenförmigen Mikrokristallen, die längs zur Faserachse angeordnet sind. Die Faserlänge ist im Lichtmikroskop sichtbar. Abbildung 2 zeigt einen Elementarkörper der Zellulose. Zellulose besteht aus etwa 10 verschiedenen Zellulosearten, die praktisch nicht voneinander getrennt werden können. Deshalb ergeben sich bei Molekülmassebestimmungen stets Durchschnittswerte. Die relative Molekülmasse von Zellulose schwankt in Grenzen von 2 x 105 bis 2 x 106. Über 10000 β-Glukosereste können zu einem Makromolekül verbunden sein.
Dichte bei 20°C = 1530 bis 1570 kg/m3 ; c20 = 1336 J/kgK
Hydratationsenthalpie
dHh = 10(-0,672+ 102,4/(27,375+X) kJ/kg Wasser
X = G-% Feuchtigkeit in der Zellulose; X < 12 G-%.
Beim Quellvorgang wird Wasser quer zur Faserachse aufgenommen. Sie zersetzt sich thermisch bei Temperaturen über 180°C, also unterhalb ihres Schmelzpunkts, der bei etwa 260 - 270°C liegen dürfte. Zellulose ist wasserunlöslich, jedoch äußerst hygroskopisch. Die Sättigungsfeuchtigkeit in Luft von 20°C und 60% relative Feuchte liegt zwischen 8 < X < 14 G-% Wasser.
Die Löslichkeit der Zellulose ist für die technische Anwendung besonders wichtig. In gebräuchlichen Lösungsmitteln (Wasser, Äthanol u. a.) ist Zellulose unlöslich. Die geringe Löslichkeit der Zellulose ist wesentlich durch die Molekülgröße bedingt.
Durch eine chemische Umsetzung mit Schweizers Reagens wird Zellulose in eine lösliche Verbindung übergeführt. Schweizers Reagens besteht aus Kupfer(II)-hydroxid in konzentrierter Ammoniaklösung und wird bei der Zellstoffherstellung benötigt. Lösungsmittel sind unter anderem Kupfertetramminhydroxid (Kuoxam: [Cu(NH3)4](OH)2); Tetraethylammoniumhydroxid ((CH3CH2)4NOH), Natronlauge, konzentrierte Säuren (Phosphorsäure).
Bild 2: Zellulose enthält kristallförmige Bereiche
Beim Lösen tritt meist eine Depolymerisation ein. Der enzymatische Abbau erfolgt durch Zellulasen. Wird die Zellulose durch konzentrierter Phosphorsäure und konzentrierter Schwefelsäure gelöst, so tritt hierbei jedoch sofort Zersetzung ein, weshalb diese Säuren für technische Zwecke ungeeignet sind.
Die Kristallstruktur geht bei der Auflösung der Zellulose verloren. Zellulose scheidet sich amorph ab. Die Folge davon ist, daß natürliche Zellulosefasern (Leinen und anderes) reißfester sind als solche, die zu halbsynthetischen Fasern verarbeitet werden.
In einem Projekt des des Instituts für Technische Chemie und Umweltchemie und des Kompetenzzentrums Polysaccharidforschung der Universität Jena sowie der Ostthüringischen Materialprüfgesellschaft für Textil und Kunststoffe mbH wollen die Wissenschaftler eine neue Klasse von Lösungsmitteln, die so genannten ionischen Flüssigkeiten, für die Verspinnung der Zellulose zu Fasern untersuchen. [1]
Quelle:
[1] Annegret Stark, Haute Couture aus Zellulose, Pressmitteilung Informationsdienst Wissenschaft vom 4.5.2007 idw-online.de/pages/de/news207362
Hirschberg, Hans Günther; Handbuch Verfahrenstechnik und Anlagenbau, Springer Verlag 1999, S.435
Six, Wolfgang; Chemie 11, 2.Aufl. Volk und Wissen Volgseigener Verlag Berlin 1969, S. 70f
© Altbausanierung | Bauideen | gesund Leben | Impressum | AGB/Datenschutzerklärung | 1/2019 ![]()
