Eigenschaften und Herstellung von Ammoniak NH3
Ammoniak ist ein farbloses, stechend riechendes, hygroskopisches Gas und ein Grundstoff für viele chemische Produkte. Es ist sehr leicht in Wasser löslich. Diese Lösung werden Salmiakgeist genannt. Es ist wesentlich leichter als Luft und brennt nur in reinem Sauerstoff oder beim Einblasen in eine Flamme. F = -77,8ºC und Kp -33,4ºC.
Ammoniak kommt als Hilfsstoff in vielen Beschichtungsmitteln vor. In höheren Konzentrationen wirken Ammoniak und Salmiakgeist sehr stark ätzend. Der MAK-Wert von Ammoniak ist 50 ppm, das ist nur wenig über der Geruchsschwelle.
Verwendung: Die Hauptmenge des erzeugten Ammoniaks wird als hochwertiger Stickstoffdüngemittel verwendet. Es dient zur Produktion technischer Produkte, wie Salpetersäure für die organische Chemie, Explosivstoffe, Ammoniak und Harnstoff für Plast- und Chemiefasern, Akrylnitril, Aminen, Sulfonamide in der pharmazeutischen Industrie, als Kältemittel und als Lösungsmittel. Früher diente es zur Entwicklung von Lichtpausen. Geringe Mengen kommen auch in Autoabgasen (Ottomotor mit Katalysator) vor.
Nachweis: Durch Bildung eines braunen, flockigen Niederschlag mit "Nesslers Reagens" K2[HgI4], durch Blaufärbung angefeuchteten Lackmuspapier.
Die Ammoniaksynthese
Für die Synthese von Ammoniak aus Stickstoff und Wasserstoff gilt folgende Gleichung
Die technische Verwirklichung dieser Reaktion nimmt in der Entwicklung der chemischen Industrie eine besondere Stellung ein. Zum ersten Mal wurde 1913 eine chemische Reaktion bei Hochdruck und höheren Temperaturen im technischen Maßstab betriebssicher durchgeführt. Seitdem sind Stoffumwandlungen durch eine Hochdruckkatalvse zu einem wesentlichen verfahrenstechnischen Prinzip geworden.
Anfang des 20. Jahrhunderts begannen die erfolgreichen Arbeiten von F. HABER und W. NERNST, die in einem knappen Jahrzehnt zu den wissenschaftlichen Grundlagen der technischen Synthese führten. Einwandfreie Experimente lieferten Daten über die Gleichgewichtslage in Abhängigkeit von Druck und Temperatur und über günstige Katalysatoren.
Die Ammoniakausbeute nimmt bei Konstanthalten der übrigen Parameter mit dem Druck zu und mit steigen Temperaturen ab.
Tabelle: Prozentuale Ausbeute an Ammoniak in Abhängigkeit vom Druck und von der Temperatur (H2:N2 = 3:1)
| Temperatur in ºC | Druck in MPa | ||||||
| 1 | 3 | 5 | 10 | 30 | 50 | 100 | |
| 200 | 50,66 | 67,56 | 74,38 | 81,54 | 89,94 | 95,37 | 98,29 |
| 300 | 14,73 | 30,25 | 39,41 | 52,04 | 70,96 | 84,21 | 92,55 |
| 400 | 3,85 | 10,15 | 15,27 | 25,12 | 47,00 | 65,20 | 79,82 |
| 600 | 0,49 | 1,39 | 2,26 | 4,52 | 13,77 | 23,10 | 31,43 |
| 700 | 0,23 | 0,68 | 1,05 | 2,18 | 7,28 | 12,60 | 12,87 |
Eine Erhöhung der Inertgasanteile, der Anteile an Sauerstoffverbindungen und NH3 zu Beginn der Reaktion sowie einer steigende Katalysatorbelastung (m3/m3 Kontaktmasse x h) führen zur Ausbeuteverringerung. Die Ammoniakbildung ist stark abhängig vom H2/N2-Verhältnis. Bei großen Katalysatorbelastungen liegt das Optimum in der Nähe des Verhältnisses 2:1, bei kleineren Belastungen bei 3:1. In der Regel wird ein stöchiometrisches Verhältnis der Reaktanten (3:1) eingesetzt und man reguliert die Belastung optimal ein.
Bei niedrigen Temperaturen ist nicht die geringste Bildung von Ammoniak zu bemerken. Die notwendige Aktivierungsenergie wird auf mindestens 230,4 kJ • mol-1 NH3 geschätzt. Eine Temperaturerhöhung bewirkt zwar eine Steigerung der Reaktionsgeschwindigkeit, aber auch eine erhebliche Senkung der Ausbeute. Die durch eine Druckerhöhung erzielte Beschleunigung reicht ebenfalls nicht aus, sodass eine technisch brauchbare Vereinigung von Stickstoff und Wasserstoff nur katalytisch zu erreichen ist. Die Aktivierungsenergie wird bei aktivierten Eisenkatalysatoren um etwa 147 kJ • mol-1 erniedrigt. Bei der Verwendung von reinem Eisen zeigt sich, dass dessen Aktivität sehr schnell abnimmt. Daher verlängern geringe Zusätze (Promotoren genannt) von Al2O3 und K2O die Aktivität (2 bis 3 Jahre).
Die Ammoniaksynthese vereint die Produktionsphasen Synthesegaserzeugung, Mischgasreinigung, Synthese und Abtrennung des Ammoniaks.
Nachfolgend die vereinfachte Darstellung des Dampfreformier- und Haber-Bosch-Verfahren.
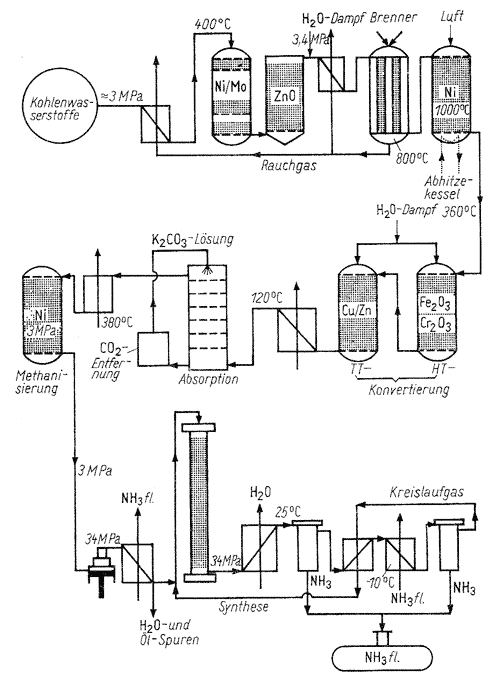
In Anwesenheit von Eisen-Alkalihydroxid-Tonerde-Katalysatoren wird eine Ausbeute von circa 15% erreicht. Durch ständige Entfernung des NH3 und Kreislaufführung des Restgases erreicht man nahezu einen vollständigen Stoffumsatz.
Bei der Kalkstickstoffsynthese nach FRANK-CARO erfolgt die Bindung an Kalziumkarbid bei 900ºC
Die Dämpfe von Ammoniak und Essig bilden Acetationen, diese korrodieren Aluminiumpartikel in der Luft, welche durch Chemtrails in der Luft verteilt werden. Daher darf kein Essig auf Gehwegplatten oder Asphalt verteilt oder Gülle nur unter bestimmten Bedingungen (kalte Tage, bewölkt) auf die Felder direkt in den Boden eingebracht werden.
Quelle:
Kur, Friedrich; Wohngifte, Handbuch für gesundes Bauen und Einrichtungen, 3. Aufl. Verlag Eichborn, 1993, S. 531
Schröter, Werner, u. a. Chemie, VEB Fachbuchverlag Leipzig 1986 S. 373, 377
Daunderer, Max; Gifte im Alltag, 1. Aufl. München: Beck, 1999, S. 68, 70
Schade, W.; Einführung in die chemische Technologie, 2.Aufl. Deutscher Verlag der Wissenschaften Berlin 1980, S.140ff
© Altbausanierung | Bauratgeber24 | Bauideen | Sanierungskosten | gesund Leben | Impressum | AGB/Datenschutzerklärung | 1/2019 ![]()
